
![]() 发布时间:2026-03-06
发布时间:2026-03-06
![]() 浏览次数:32
浏览次数:32
3月6日,是世界淋巴水肿日。血管生成是从已有血管新生血管的过程,参与损伤修复、炎症与肿瘤进展;淋巴管生成则是胚胎期淋巴管网络形成与扩展的核心机制,也是肿瘤细胞进入淋巴系统的关键过程。异常的血管、淋巴管生成,常常会引起炎症性皮肤病、淋巴水肿、硬皮病、肥胖、高血压、肿瘤转移等各类疾病。
近年来,斑马鱼凭借其独特的优势,已从单纯观察淋巴管和血管生成、发育,发展成为可以深入探究“基因-细胞-功能-药物”多维关系的综合性研究平台,为探究血管/淋巴调控机制、靶向调控异常淋巴管及血管生成、干预炎症性疾病、心血管病及肿瘤等疾病进展提供了全新的工具。目前,环特生物已开发血管/淋巴相关转基因品系斑马鱼、斑马鱼淋巴损伤等系列模型,并可以为客户开展血管/淋巴相关课题方案设计,欢迎有需要的客户垂询!
01、斑马鱼在淋巴/血管生成中的应用进展
斑马鱼淋巴管形成和发育周期较短,具有体外发育、胚胎透明、清晰易观察等优势,是淋巴管、血管生成研究领域理想的动物模型。
基于转基因品系斑马鱼模型,不仅可以实时追踪淋巴管、血管形成及重塑过程,深入解析VEGFs、血管生成素等信号通路的分子网络,而且,能可靠模拟淋巴/血管生成异常导致的各类疾病,直观观察巨噬细胞、中性粒细胞等免疫细胞与脉管系统的动态互作,揭示炎症微环境对血管生成的调控机制,使其在淋巴/血管发育机制、疾病治疗与机制解析、中药现代化研究、调控机制研究等领域展现出卓越的价值。
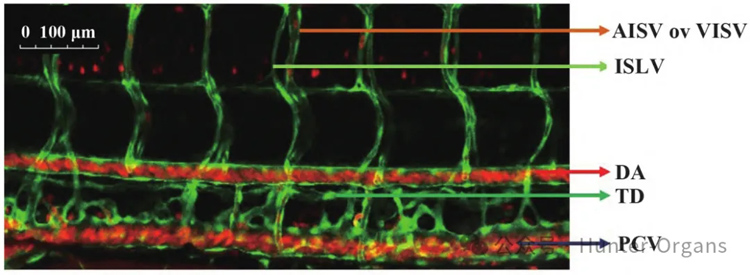
图1 转基因斑马鱼(gata1:DsRed;fli1:EGFP)的血管和淋巴管,来源:陈岩, 等. 斑马鱼模型淋巴系统研究进展[J]. 中国免疫学杂志, 2022, 38(11): 1396-1400.
一、斑马鱼:发育机制的“活体显微镜”
1. 淋巴系统发育:斑马鱼可用于揭示淋巴管起源,连接"基因-细胞-功能"研究、解析淋巴系统发育机制及探索相关疾病干预靶点等。2025年底,Nat Rev Mol Cell Bio.上一项最新研究,通过斑马鱼模型揭示了VEGFR3–PROX1轴在淋巴管发育中的必要性;也有研究发现凝血酶受体Parl能调控斑马鱼淋巴管发育,并揭示了发育关键因子VEGF-C/VEGFR3、CCBE1、CXCL12/CXCR4等,以及躯干、肠道、面部等不同部位的淋巴管遗传异质性方面的核心作用。
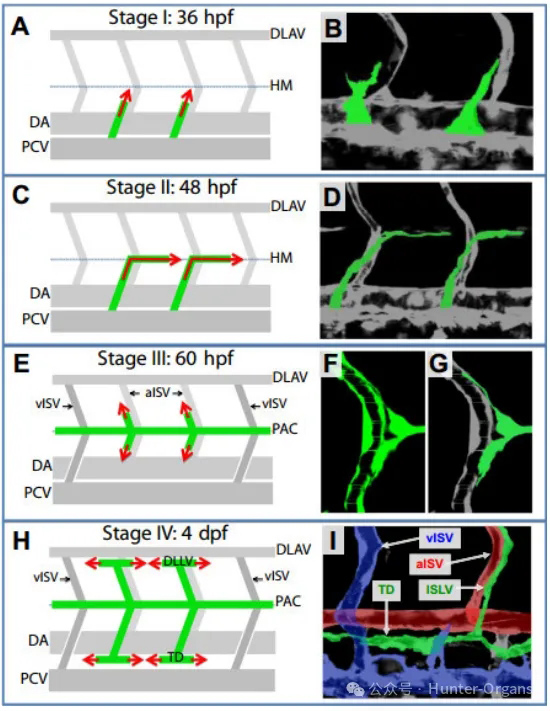
图2 斑马鱼躯干淋巴管发育的阶段(TS Mulligan & BM Weinstein. Microvas Res. 2014 )
2. 血管系统发育:斑马鱼也是研究血管生成与再生的理想模型,其躯干节间血管(ISV)已成为筛选促/抗血管生成药物的经典评价指标。已有研究利用斑马鱼鳍再生实验,证明了在组织再生的生理性血管形成过程中,存在一个与肿瘤血管拟态非常相似的过程,并明确了VEGFA/VEGFR2信号轴在血管出芽、迁移及管腔形成中的核心驱动作用,揭示了Notch、Wnt及凝血酶受体Parl等信号通路对血管新生时空秩序的精细调控;2025年,法国留尼旺大学Nicolas Diotel团队首次在生理/组织学层面证明了斑马鱼血管再生与神经发生之间的相关性。
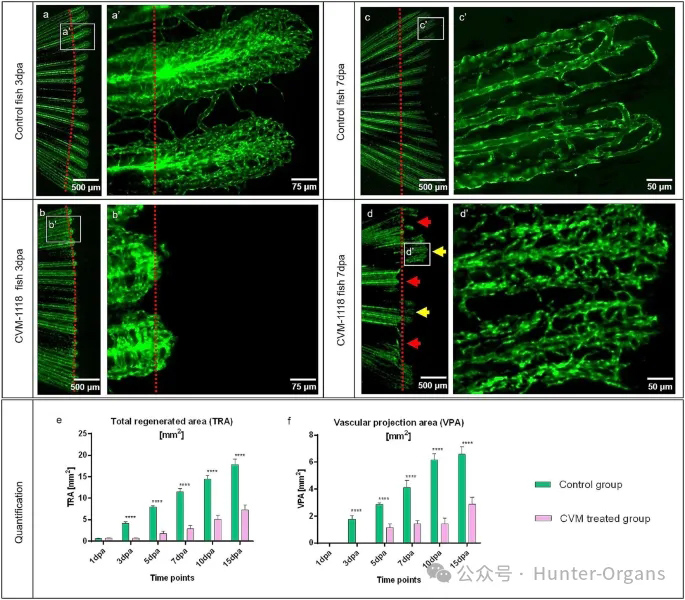
图3 血管拟态抑制剂CVM - 1118抑制斑马鱼尾鳍再生血管生成,Angiogenesis,2024.3.
二、斑马鱼:人类疾病的“替身”与机制解析平台
1. 炎症性疾病研究:斑马鱼保留了复杂的免疫系统和相关基因表达,为研究炎症性疾病与淋巴管的相互作用提供了直观的实验平台。已有研究利用斑马鱼炎症性肠病(IBD)模型(DSS 诱导),首次在斑马鱼中揭示了IL-22/TGF-β/Mmp9 信号轴在IBD中的关键作用;也有研究表明,激活斑马鱼VEGFR3信号转导可促进心脏再生和炎症消退,揭示了巨噬细胞通过分泌VEGFs驱动炎症性淋巴管新生的细胞机制。
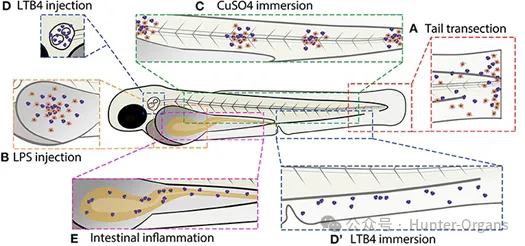
图4 常用斑马鱼炎症模型示意图,Zanandrea R,et al. Drug Discov Today. 2020 Dec;25(12):2201-2211.
2. 心血管疾病:斑马鱼模型在心血管疾病研究中具有不可替代的优势,为疾病机制探索、药物研发和再生医学研究提供了重要平台。已有研究首次构建出斑马鱼心脏再生全过程的高分辨率时空动态图谱,也有研究将扩张型心肌病(DCM)与心脏淋巴管新生障碍联系起来,并有多项研究证实中药及活性成分可促进斑马鱼血管新生,如丹酚酸B、阿魏酸通过调节VEGF信号传导发挥作用;异甜菊醇、山参和园参的血管生成活性与缺氧诱导因子-1α/VEGF信号传导相关。
3. 脑血管疾病:已有研究构建了斑马鱼脑血管发育时空图谱,揭示了内皮细胞异质性及血脑屏障调控新基因;也有研究发现,脑膜淋巴管能侵入脑实质,作为“生长轨道”引导新生血管,并清除脑水肿液,为理解脑卒中后修复机制和开发新疗法提供了全新视角;而“神经-胶质-成纤维细胞”调控轴的揭示,则表明神经活动可通过放射状星形胶质细胞动态调控Vegfc表达,精准调控脑膜淋巴内皮细胞(muLECs)的发育。
4. 免疫系统再生:斑马鱼作为研究免疫系统再生的模型生物,其保守的免疫和致癌信号通路,使得在体内对肿瘤-免疫相互作用进行高分辨率、实时成像成为可能,共同推动组织再生。已有研究针对斑马鱼胸腺淋巴细胞损伤后再生机制,构建了斑马鱼胸腺损伤模型,揭示了CXCL12b/CXCR4b信号轴引导造血前体细胞迁移至胸腺,实现T细胞再生的关键作用,对免疫缺陷病治疗有重大意义。
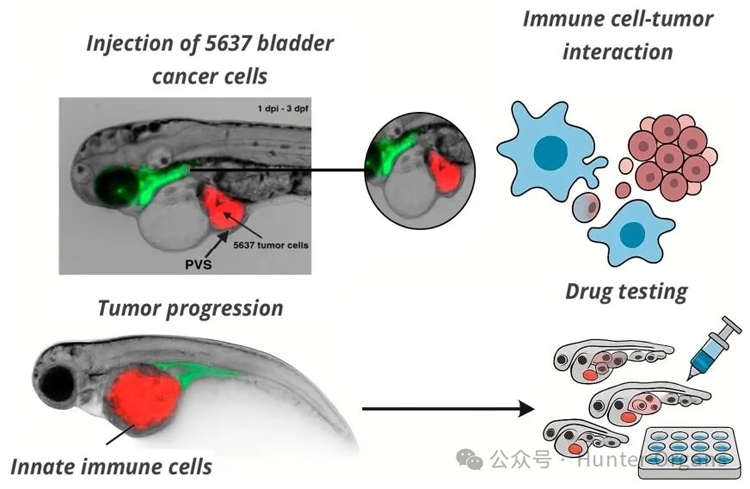
图5 斑马鱼异种移植模型中肿瘤-免疫相互作用
三、斑马鱼:中药现代化研究的“加速器”
斑马鱼凭借高通量、直观可视及成本低等优势,可同时评价促淋巴管/血管生成等药效指标,发育、心脏等多器官毒性等,完美契合中药“多成分、多靶点、整体调节”的研究特点。
已有多项研究证实了中药的调控潜力:扩心方及其主要成分丹酚酸B通过上调VEGF-C/VEGFR-3表达促进淋巴管生成,改善扩张型心肌病;三七总皂苷经ERK、PI3K及p38 MAPK信号通路上调VEGF-C,发挥促淋巴作用;独活寄生汤可促进胸导管形成并改善淋巴引流功能;苓桂术甘汤则通过IL-17通路调控淋巴管生成,首次利用斑马鱼证实“促进淋巴管生成”是LD改善心肌重构的必要且充分条件,为心梗治疗提供新策略;苦玄参在缓解代谢性炎症中的机理也通过斑马鱼模型得以揭示。
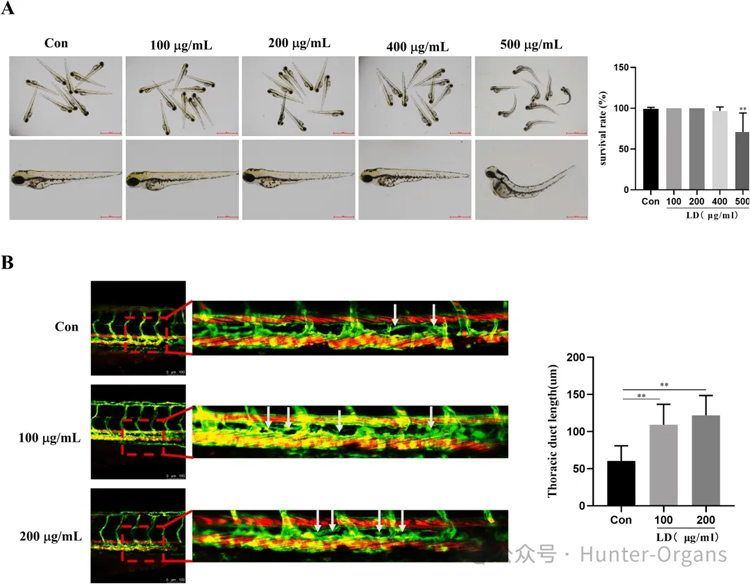
图6 淋巴管生成是LD改善斑马鱼心肌重构的重要途径
此外,斑马鱼正与网络药理学深度融合,通过预测靶点后,借助基因敲降/敲除、抑制剂及转基因品系进行验证,形成了“预测-验证”的闭环研究体系,为中药活性成分筛选、药效验证及机制解析提供了高效平台。
四、斑马鱼:信号通路的“体内验证场”
斑马鱼凭借其活体成像与遗传操作优势,能够研究关键基因与信号通路在血管、淋巴生成中的调控作用,已成为解析血管与淋巴系统信号通路的理想平台。已有许多研究利用斑马鱼模型,聚焦于以VEGF家族(VEGF-A、-C、-D)及其受体(VEGFR2、VEGFR3)为核心的调控轴,同时涉及CXCL12/CXCR4趋化因子信号、G蛋白偶联受体及MAPK/ERK级联反应等多条通路的协同参与。
这些通路在不同生理和炎症、损伤等病理背景下,被很多研究反复验证,不仅揭示了相关关键信号通路在血管生成与淋巴管形成中的核心地位,也为解析中药复方及活性成分的作用靶点、筛选通路特异性调节剂提供了兼具高通量与高内涵的“体内验证场”。
02、淋巴/血管核心标记物及转基因品系斑马鱼
淋巴管标志通常指的是淋巴内皮细胞特异性的标志物,LYVE-1、podoplanin、Prox1和VEGFR-3等是最常用于淋巴管显微成像的核心标记物。
淋巴/血管的关键信号轴包括:
1. VEGF-C/VEGFR3:驱动淋巴管生成的最核心通路;
2. VEGFA/VEGFR2:驱动血管生成的最核心通路;
3. CXCL12/CXCR4:引导细胞,如淋巴管前体细胞、造血前体细胞等迁移的关键趋化信号;
4. Angiopoietin/Tie:参与血管和淋巴管成熟与稳定。
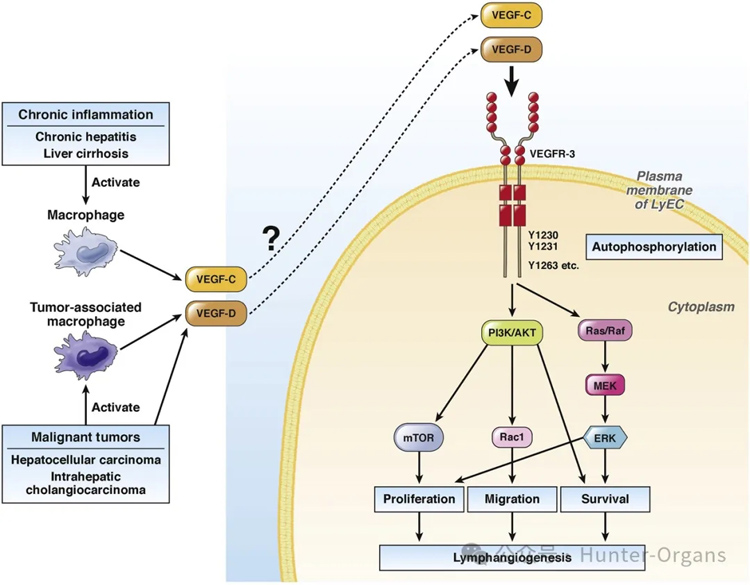
图7 淋巴管生成的细胞内信号传导途径
一些主要的细胞类型:
1. 淋巴管内皮细胞(LECs):淋巴管的基本构成单位;
2. 巨噬细胞(Macrophages):在炎症条件下,可分泌VEGF-C/A促进淋巴管/血管新生,是连接炎症和淋巴管新生的关键纽带;
3. 造血前体细胞(HSPCs):在胸腺损伤后,其从肾脏(相当于哺乳动物的骨髓)迁移至胸腺,分化为T细胞。
常用的转基因品系斑马鱼:
1. Tg(fli1:EGFP)转基因品系:观察斑马鱼血管最成熟的品系,eGFP在体节发生早期就可在侧板中胚层被检测到,且其表达持续存在于所有血管、造血细胞类型以及颌间充质中;
2. Tg(flk1:EGFP/DsRedEx):血管内皮标记;
3. Tg(lyve1b:DsRed2) sj319Tg:淋巴管(及部分静脉)标记;
4. Tg(mpeg1:EGFP)巨噬细胞转基因品系;
5. Tg(mpx:GFP)中性粒细胞转基因品系。
03、淋巴/血管课题方案设计思路
示例课题:探究某中药单体X对心肌梗死后的淋巴管新生及心功能保护作用
背景:心梗后心肌水肿、炎症和纤维化是导致心衰的主要原因。淋巴管能清除水肿和炎症因子,促进修复。已有研究表明促进淋巴管新生可改善心功能。
研究目标:明确中药单体X是否能促进心梗后淋巴管新生,并改善心功能。
实验设计:
1.体外筛选:在人淋巴管内皮细胞(HDLEC)上,检测单体X对细胞增殖(CCK-8)、迁移(划痕实验)和成管能力的影响;Western Blot/qPCR检测其对VEGF-C、VEGFR3、PROX1等淋巴管生成关键蛋白/基因表达的影响。
2. 斑马鱼模型验证(核心):
(1)模型构建:利用Tg(lyve1b:DsRed2) sj319Tg或Tg(fli1:EGFP; gata1:DsRed)斑马鱼构建模型;
(2)损伤诱导:使用斑马鱼心肌特异性损伤模型(如Tg(cmlc2:eGFP)品系,通过异丙肾上腺素诱导心肌细胞凋亡,模拟心梗或更通用的VEGFR3抑制剂MAZ51诱导躯干淋巴管损伤。
3. 给药与分组:设置对照组、模型组、单体X低/中/高剂量组、阳性药组,如重组VEGF-C蛋白);
4. 药效评价:
(1)淋巴管新生:共聚焦显微镜观察并量化心脏区域(或躯干TD)的淋巴管数量、长度和覆盖率;
(2)心功能评价:通过测量心室收缩舒张面积、心率等指标,评估心功能改善情况;
(3)水肿与炎症:观察心包水肿面积,利用中性粒细胞(mpx:EGFP)或巨噬细胞(mpeg1:EGFP)转基因系,评估炎症细胞浸润情况。
5. 机制验证:
(1)RT-PCR检测整体斑马鱼中vegfc、vegfr3、prox1a、vegfa等mRNA水平;
(2)利用VEGFR3抑制剂(如MAZ51)进行挽救实验,验证单体X的作用是否依赖于VEGFR3通路。
目前,环特已建立斑马鱼淋巴/血管等系列模型及200多种各类疾病斑马鱼模型,脑类器官、心脏类器官及各种肿瘤类器官培养平台,并利用积累深厚的基因编辑技术,为医生和科研工作者提供疾病模型构建、发病机制研究、分子标志物与靶点发现和安全性研究等多种疾病的深度科研服务,内容涵盖从课题项目咨询、实验方案设计、实验开展、数据整理分析等一系列全面技术支持,欢迎有需要的读者垂询!